
Eine Nahaufnahme einer Mücke auf einem weißen Hintergrund.
Moskito-Management: Forscherteam setzte Gen-Gelsen frei
Vorige Woche startete die nächste Projektphase: Da platzierten Mitarbeiterinnen und Mitarbeiter des Biotech-Unternehmens Oxitec sechseckige Behältnisse in drei Regionen Floridas. „Moskito-Boxen“ nennt das britische Start-up diese Gefäße. Bereits im Vorjahr waren solche Konstruktionen das Herzstück eines großen Feldversuchs, dessen Ergebnisse kürzlich im Fachjournal „Nature“ erläutert wurden. Es war eine Studie mit Erregungspotenzial: Denn Oxitec hatte erstmals in den Vereinigten Staaten gentechnisch veränderte Stechmücken freigesetzt.
Fünf Millionen Exemplare der Gelsenart Aedes aegypti wurden ab April 2021 über sieben Monate an ausgewählten Orten Floridas in die Natur entlassen – wenn auch unter kontrollierten Bedingungen: Der Versuch fand unter behördlicher Aufsicht auf Privatgrundstücken statt, um das Versuchsgebiet räumlich zu begrenzen. Ziel des Experiments war der Test neuer molekularbiologischer Methoden zur Dezimierung der Gelsenpopulationen. Die Idee dahinter: Auf diesem Weg könnte es gelingen, die Verbreitung übertragbarer Erkrankungen einzudämmen.
Denn wie viele Moskitos kann Aedes aegypti, die Ägyptische Tigermücke, als sogenannter Vektor für zahlreiche Viren dienen, also beim Blutsaugen Krankheitserreger auch auf den Menschen übertragen. Zu diesen Erregern zählen Dengue-, Gelbfieber-, Zika- und Chikungunya-Viren. Sehr oft verursachen sie harmlose Infekte, manchmal aber auch gravierende Erkrankungen. Vor rund fünf Jahren stellte sich im Zuge einer Zika-Epidemie in Südamerika heraus, dass das Virus ungeborene Kinder schwer schädigen kann. Dengue wiederum kann bei einem kleinen Prozentsatz der Infizierten zu Komplikationen wie Blutungen und in sehr seltenen Fällen sogar zum Tod führen. Bis zu einer halben Milliarde Menschen weltweit fängt sich jedes Jahr das Dengue-Virus ein.
Einst auf tropische und subtropische Gebiete beschränkt, breiten sich Aedes-Arten mittlerweile über den Globus aus: vor allem aufgrund des internationalen Güterverkehrs und des Klimawandels. Aedes aegypti ist zwar in Europa noch kein Thema, wohl aber in den USA, besonders im Süden. Deshalb fanden und finden die ersten amerikanischen Pilotversuche in Florida statt. „Nature“ beschrieb nun im Detail, wie die Methode funktioniert: Das Forscherteam schleuste im Labor ein spezielles Gen in männliche Gelsen ein. Dieses Gen ist tödlich für den weiblichen Nachwuchs – und zwar ausschließlich für die Weibchen. Nur diese saugen Blut und können dadurch Viren übertragen.
Einmal freigesetzt, sollen sich die gentechnisch veränderten Männchen mit wilden Weibchen paaren, und deren weiblicher Nachwuchs stirbt ab, bevor er sich seinerseits reproduzieren kann. Die Männchen hingegen können sich weiter fortpflanzen. So wiederholt sich der Vorgang von Generation zu Generation, sodass mit jeder davon weniger Weibchen übrig bleiben – und die Mückenpopulation insgesamt schrumpft. Allerdings verbleibt das letale Gen nicht dauerhaft in der Umwelt: Nach einigen Generationen verschwindet es von selbst, sodass die genetische Manipulation nicht Bestand hat.
Aus rein wissenschaftlicher Sicht scheint das Experiment erfolgreich gewesen zu sein: Die Oxitec-Forschenden sammelten im Versuchsareal gut 22.000 Eier ein und studierten sie im Labor. Resultat: Alle Weibchen, die das eingeschleuste Gen in sich trugen, starben vor dem reproduktionsfähigen Alter. Ob das letale Gen tatsächlich vorhanden war, ließ sich mittels Fluoreszenz überprüfen: mithilfe einer leuchtenden Substanz, die samt dem Gen transferiert wurde und die wie ein molekularbiologischer Marker wirkt.
Die Methode dürfte somit ihren Zweck erfüllen. Eine ganz andere Frage ist, inwiefern sie ethisch vertretbar ist. Darf man genetisch manipulierte Insekten einfach in die Natur entlassen? Kann dies unerwünschte oder gar unkontrollierbare Konsequenzen haben? Vertreter von Umweltschutzorganisationen und Gegner der Gentechnik protestierten jedenfalls umgehend gegen die Feldversuche.
Wie bedenklich sind die Experimente aber tatsächlich? „Eigentlich gibt es kaum einen Grund zur Skepsis“, meint der Wiener Virologe Norbert Nowotny, der sich an seinem Institut an der Veterinärmedizinischen Universität seit Langem mit durch Moskitos übertragenen Erregern befasst. Es bestehe mitunter zwar die Befürchtung, dass das eingeschleuste Gen auf andere Insekten übergehen könnte, so Nowotny. Doch das sei ein sehr theoretisches Szenario, da sich Gelsen nicht einfach mit anderen Insektenarten paaren können. Viel eher denkbar sei eine „Rückentwicklung zum Normalzustand“: dass das Fremdgen früher als beabsichtigt aus den Populationen verschwindet. Dann würden freilich bloß wieder herkömmliche Moskitos durch die Gegend surren. Grundsätzlich sei dennoch verständlich, dass viele Menschen Unbehagen beschleiche bei der Vorstellung, genetisch manipulierte Organismen in die Natur zu entlassen. Schließlich habe man dann praktisch keinen Einfluss mehr darauf.
Weiters könnte man die Frage stellen, ob eine Dezimierung der Gelsenbestände auch ökologische Nachteile mit sich bringt. Das ist tatsächlich der Fall: „Sie sind ein Glied der Nahrungskette und beispielsweise für Frösche wichtig“, sagt Nowotny. Um einen Eingriff in die Natur handle es sich somit auf jeden Fall. Allerdings: Es steht außer Zweifel, dass „vector-borne diseases“ – durch Stechmücken übertragene Infektionskrankheiten – zunehmend zum Problem werden, weil sich die Insekten wie auch ihre virale Last immer mehr in Weltregionen ausbreiten, in denen sie vormals nicht heimisch waren. Zwar ist es sehr unwahrscheinlich, dass die nächste Pandemie durch Moskitos ausgelöst werden könnte, wie die „Los Angeles Times“ vor einiger Zeit mutmaßte, doch ist es plausibel, anzunehmen, dass sich lokale Ausbrüche und Epidemien künftig häufen. Die Dimension solcher Ereignisse kann durchaus beachtlich sein: So führte ein Chikungunya-Ausbruch in der Karibik vor knapp zehn Jahren zu Hunderttausenden Infizierten.
Daraus resultiert auch die Notwendigkeit zu Strategien gegen die Krankheitsvektoren. Traditionell setzte man oft auf Pestizide, doch diese haben sich kaum bewährt. Erstens handelt es sich schlicht um toxische Chemie, zweitens scheinen Stechmücken die Gefahr zu erkennen und ihr auszuweichen. Erst im Februar zeigten Experimente der Johns Hopkins University, dass sich Moskitos den Geruch von Pestiziden gut merken und damit kontaminierte Orte meiden. Je nach Spezies gelang dies bis zu fast 90 Prozent der Insekten. Giftige Chemie kommt daher einer wenig effizienten Schrotflinte gleich. Das Forschungsteam war durchaus beeindruckt von den olfaktorischen Fähigkeiten und konstatierte: Man müsse sich von der Vorstellung verabschieden, dass Gelsen bloß „fliegende Stachel“ seien.
Weil bisherige Methoden kaum greifen, setzt man heute auch auf Gentechnik. Oxitec erhielt nun die Bewilligung für weitere Freilandstudien, die soeben starteten, und in Mexiko und Brasilien wurden bereits ähnliche Studien durchgeführt. Angeblich konnten die Bestände von Aedes aegypti dort um bis zu 95 Prozent reduziert werden. Auch in Österreich liefen Versuche mit Methoden, die den Gelsennachwuchs unterbinden sollen. Vor einigen Jahren trachteten Forschende der Internationalen Atomenergiebehörde in Seibersdorf danach, Männchen mit ionisierender Strahlung zu sterilisieren. Derart war angedacht, das Zika-Virus an der Verbreitung zu hindern.
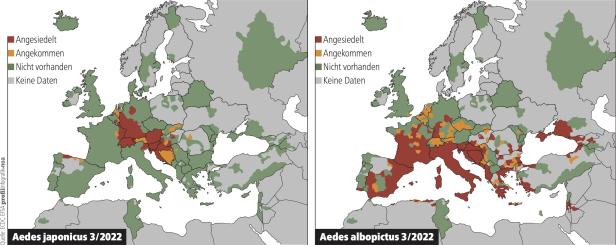
Der Stechmücken-Atlas
Die Karten zeigen die Verbreitung zweier vormals exotischer Gelsenarten, die in Europa nun immer häufiger vorkommen. Die Asiatische Buschmücke (links) ist in allen Bundesländern Österreichs verbreitet. Die Asiatische Tigermücke (rechts) ist bei uns noch seltener, aber europaweit bereits etabliert.
Die Arbeiten zielten freilich nicht auf einen Einsatz in Österreich ab. Doch auch hier und allgemein in Europa werden „mosquito-borne diseases“ zunehmend relevant – wobei man zwischen vermehrtem Auftreten exotischer Gelsen und
Viren unterscheiden muss, die bei uns früher praktisch nicht vorkamen (siehe Karten oben). Seit Jahren überwachen Expertenteams die Situation, darunter Wissenschaftergruppen an Nowotnys Institut, dem Zentrum für Virologie an der Medizinischen Universität Wien, sowie der Agentur für Gesundheit und Ernährungssicherheit (AGES).
Während sich Aedes aegypti bei uns noch nicht ansiedeln konnte, weil die Temperaturen vorerst nicht hoch genug sind, ist ein Verwandter am besten Weg dazu: Aedes albopictus, die Asiatische Tigermücke. „Sie hat ein ähnliches Erregerpotenzial wie Aedes aegypti, ist aber eine Spur weniger gefährlich“, sagt Nowotny. Eine Begegnung mit einer infizierten Gelse kann dennoch unerfreulich enden: Die Tigermücke kann mehr als 20 Infektionskrankheiten hervorrufen, darunter West-Nil-Fieber, Dengue, Gelbfieber und Chikungunya. Nachweise dieser Insekten gibt es in gesamt Mittel- und Südeuropa, sehr viele davon in Südtirol.
Die Mechanismen der Ansiedelung sind stets ähnlich: Durch den internationalen Frachtverkehr, etwa an Bord von Sattelschleppern, gelangen die Gelsen ins Land, das immer wärmere Klima erlaubt dann die dauerhafte Etablierung. Dies ist zum Beispiel der Mückenart Aedes japonicus bereits gelungen: Die Asiatische Buschmücke ist heute in Österreich in allen Bundesländern verbreitet. Zum Glück ist ihr Spektrum an Krankheitserregern – etwa das West-Nil- und das Usutu-Virus – geringer als jenes mancher ihrer Kolleginnen. Das lässt sich relativ präzise angeben, weil jede Gelsenart ausschließlich auf bestimmte Viren spezialisiert ist und nur diese überträgt.
Eine separate Geschichte sind einst tropische Krankheitserreger, die mittlerweile auch in unseren Breiten aufgespürt werden. Zu unterscheiden sind sie deshalb, weil sie keine exotischen Moskitos benötigen, um sich zu verbreiten. Dazu genügt Culex pipiens vollauf: die Gemeine und uns lang vertraute Hausgelse. Sie kann sich solche Viren beispielsweise einfangen, wenn sie bei Zugvögeln Blut saugt – und anschließend die Erreger an ein menschliches Opfer weiterreichen. Ein anderer Weg der Einschleppung sind Touristen, die Viren von Reisen mitbringen. Sie können zwar keine weiteren Menschen anstecken, schlagen sich aber in der Fallstatistik nieder, wenn bei ihnen bestimmte Viren nachgewiesen werden, etwa beim Blutspenden.
Daten liegen inzwischen zum Beispiel für das West-Nil- und das Usutu-Virus vor. Ersteres ist traditionell unter anderem in Afrika, im Mittleren Osten, in Indien und seit der Jahrtausendwende in Amerika heimisch – wird aber seit 2009 auch in Österreich registriert. Die Fallzahlen sind zum Glück noch sehr gering: Bis zum Vorjahr wurden laut AGES 52 Personen erfasst, die sich das Virus im Inland eingefangen hatten, also vermutlich durch infizierte Gelsen. Die Ansteckungsorte konzentrierten sich auf den Osten des Landes: Wien, Niederösterreich und das Burgenland. Besonders viele West-Nil-Virus-Infizierte gab es mit 27 Fällen im Sommer 2018. Noch deutlich seltener betrifft ein enger Verwandter dieses Virus den Menschen: das Usutu-Virus, das allerdings immer wieder unter Vögeln wütet und mehrmals zu einem Amselsterben geführt hat.
Dass die bisher registrierten Infektionen vermutlich nur die Vorboten einer erwartbaren Entwicklung sind, gilt unter Fachleuten jedoch als ziemlich wahrscheinlich. Denn wenn parallel zueinander mehr gebietsfremde Vektoren wie auch exotische Viren auftreten, erhöht dies in Kombination eines Tages auch das Risiko neuer Infektionsketten. Ob sich dem Problem künftig mittels Gentechnik oder anderer Methoden beikommen lässt, ist freilich ungewiss. Im Moment bleiben die klassischen Werkzeuge der Gelsenabwehr: Gelsensprays, Mittel zum Einreiben, lange Ärmel und Hosenbeine.


